São Paulo não registra intercorrência a lotes suspensos da CoronaVac
O governador de São Paulo, João Doria, disse hoje (8) que o estado não registrou qualquer intercorrência relacionada aos lotes da vacina CoronaVac que foram suspensos pela Agência Nacional de Vigilância Sanitária (Anvisa), ou seja, ele disse que não foram detectados quaisquer sintomas adversos nas pessoas que tomaram esse imunizante. Antes da suspensão, São Paulo já havia distribuído 4 milhões de doses desse imunizante.

Desse total, 224.737 doses ainda não foram aplicadas e vão permanecer armazenadas até que a Anvisa analise e libere esses lotes.
A CoronaVac é uma vacina que está sendo produzida pelo Instituto Butantan e o laboratório chinês Sinovac e é aplicada em duas doses.
Segundo o governo paulista, a Secretaria estadual da Saúde está monitorando os pacientes que tomaram a vacina CoronaVac desses lotes que foram suspensos pela Anvisa.
As pessoas que receberam essas doses, de acordo com o governo de São Paulo, vão ser observadas por 30 dias como medida preventiva.
De acordo com o governo paulista, antes da distribuição para a população, essas doses passaram por rigoroso controle de qualidade e foram certificadas pelo Instituto Nacional de Controle de Qualidade (INCQS), órgão da Fiocruz, responsável pela avaliação da qualidade de todos os imunizantes distribuídos no Brasil. As vacinas foram validadas e, portanto, tiveram a qualidade garantida para a utilização na população.
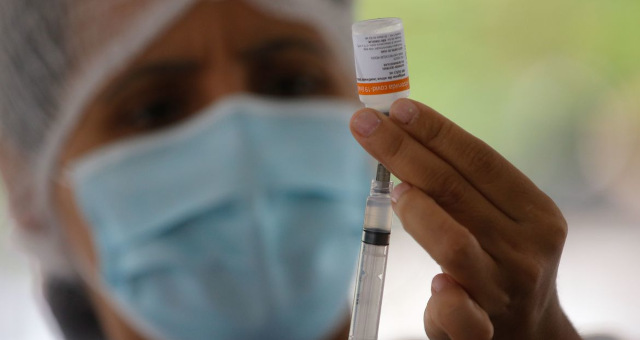
O diretor do Instituto Butantan, Dimas Covas, tranquilizou a população informando que essas doses aplicadas dos lotes que foram suspensos pela Anvisa não oferecem riscos à população. “Esses lotes foram produzidos na fabrica da Sinovac que produz todas as vacinas, submetido ao controle de qualidade, e todas as unidades são credenciadas pela Anvisa. O que ocorreu é que a Sinovac colocou em funcionamento várias linhas de envase. As vacinas são produzidas em um local e envasadas em outro. Esse lote foi envasado em uma das fábricas novas, que não havia sido visitado [pela Anvisa]”, explicou Covas.
“Isso criou uma necessidade de acertar a certificação dessa nova unidade. Isso está sendo providenciado, a documentação providenciada. A Anvisa aguarda a chegada do documento da agência sanitária chinesa. Isso deve chegar ainda antes do final dessa semana. Do ponto de vista da qualidade e segurança, não existe dúvida. Foi atestada pelo laboratório de qualidade da Sinovac na China, que é referendado pela Anvisa, testado pelo Butantan, que faz o controle de qualidade, e atestado pelo INCQS, que controla a qualidade de vacinas no Brasil. Não há questionamentos no momento sobre a qualidade e segurança das vacinas”.
Suspensão
No dia 4 de setembro, a Anvisa interditou cautelarmente 25 lotes da vacina CoronaVac, com um total de 12.113.934 de doses do imunizante. Outros 17 lotes envasados no mesmo local, com 9 milhões de doses, estão em tramitação de envio e liberação ao Brasil.
Segundo o Butantan, foi o próprio instituto quem avisou a Anvisa sobre esses lotes, que foram envasados em um local que ainda não foi inspecionado pela agência brasileira. Por isso, a aplicação de doses desses lotes foram suspensos temporariamente, até que sejam atestadas a qualidade do local onde essas vacinas foram envasadas.
“Nosso controle de qualidade percebeu mudança no padrão. Entramos em contato com a Sinovac e imediatamente comunicamos a Anvisa, que fez a interdição cautelar. A partir dai, começamos a trabalhar com a Anvisa para liberar esses doses”, explicou Rui Curi, diretor-executivo do Butantan. “A vacina tem um controle de qualidade rigoroso, como todo o resto da fábrica. É uma questão apenas de formalização dessa linha de envase”, explicou.
A interdição cautelar tem o prazo de 90 dias. A Anvisa informou que, durante esse período, “trabalhará na avaliação das condições de boas práticas de fabricação da planta fabril não aprovada, no potencial impacto dessa alteração de local nos requisitos de qualidade, segurança e eficácia, e do eventual impacto para as pessoas que foram vacinadas com esse lote”.



![[Conteúdos gratuitos] Assista ao Giro do Mercado e outros programas exclusivos em nosso Youtube](https://www.moneytimes.com.br/uploads/2024/01/banner-html-28.png)








